宮園 浩平教授
大学院医学系研究科 病因・病理学専攻
SDGs
連携提案
当研究室はがんを中心に病気の原因を明らかにし、新たな治療法を見いだすために研究を行うことを目的としている。
TGF-β(transforming growth factor-beta)が腫瘍抑制作用を失い腫瘍促進因子として作用するように変化する分子機構を明らかにし、かつTGF-βが持つ多彩な腫瘍促進作用を解明することを目指しており、以下のような研究テーマに取り組んでいる。
(1) TGF-β-Smadのダイナミックな転写調節機構の解明
(2) TGF-βによる上皮間葉転換(EMT)の調節機構と多彩な表現型の解析
(3) がんの浸潤・転移を促進するTGF-βの多彩な作用の解明
最近の新たな研究成果としては、以下の3つが挙げられる。
(a) 組織透明化手法を用いたがんの浸潤転移機構の解明
(b) 新規ミオスタチン阻害薬である 1 価 FSTL3-Fc の開発
(c) Mesenchymal型神経膠芽腫に対する新規治療法の開発
これらの研究の応用、治療法開発に関心のある企業との連携を希望する。
事業化プロポーザル
-
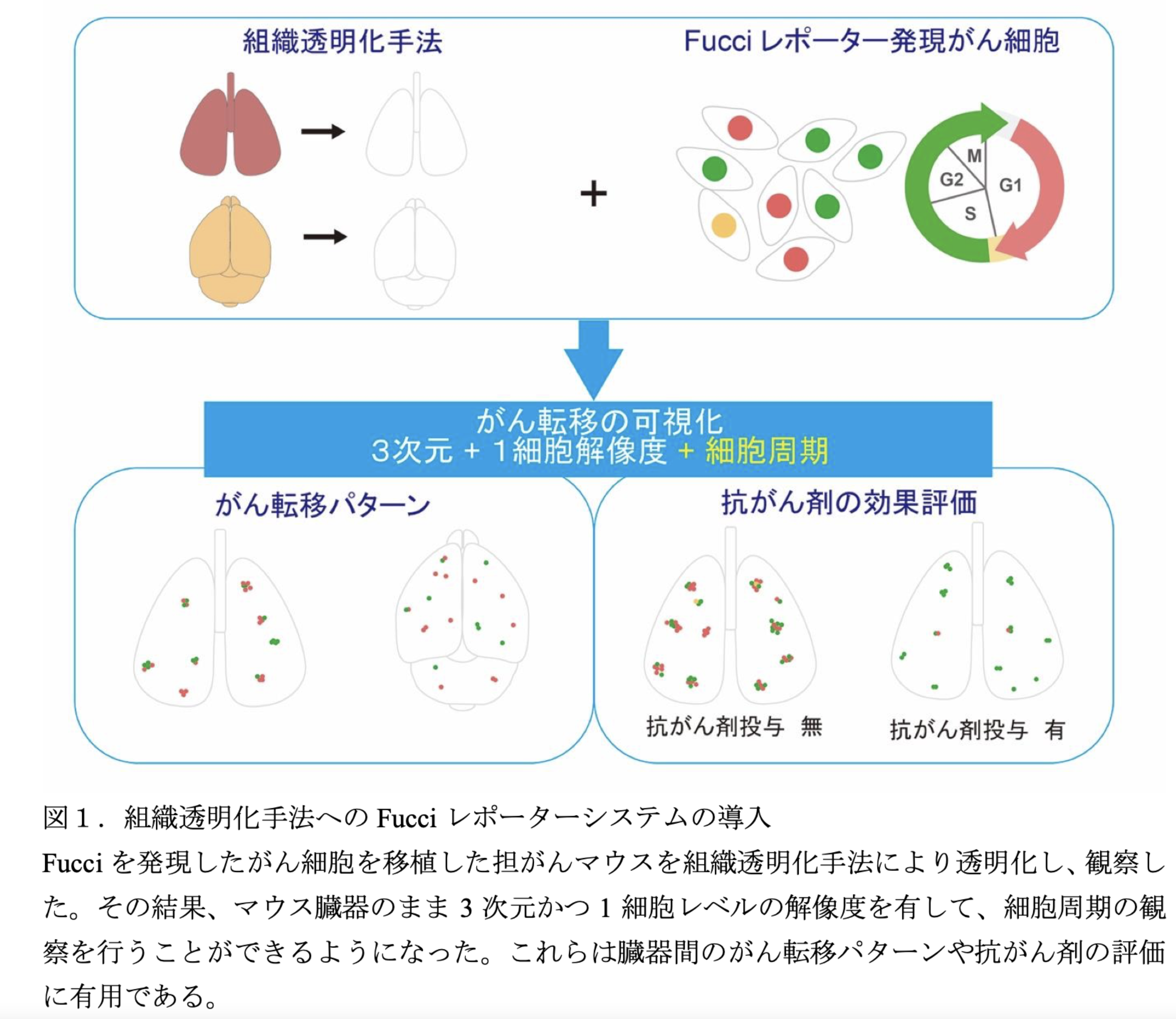 組織透明化手法と細胞周期観察蛍光プローブを組み合わせ、がん転移と抗がん剤耐性機構の解明に有用なイメージング手法を確立組織透明化手法と細胞周期を観察することができる蛍光プローブ Fucci(フーチ)を組み合わせることで、マウス臓器内のがん転移を臓器のまま、3 次元かつ 1 細胞解像度を有して、細胞周期を観察する系を立ち上げました。 転移先臓器の違いによりがん転移の形や大きさ、細胞周期パターンに違いがあるだけでなく、同一臓器内のがん転移巣の間でも腫瘍の細胞周期パターンに違いがあることが示唆されました。 本手法はがん転移の臓器指向性や抗がん剤耐性メカニズム解析に今後活用されることが期待されます。
組織透明化手法と細胞周期観察蛍光プローブを組み合わせ、がん転移と抗がん剤耐性機構の解明に有用なイメージング手法を確立組織透明化手法と細胞周期を観察することができる蛍光プローブ Fucci(フーチ)を組み合わせることで、マウス臓器内のがん転移を臓器のまま、3 次元かつ 1 細胞解像度を有して、細胞周期を観察する系を立ち上げました。 転移先臓器の違いによりがん転移の形や大きさ、細胞周期パターンに違いがあるだけでなく、同一臓器内のがん転移巣の間でも腫瘍の細胞周期パターンに違いがあることが示唆されました。 本手法はがん転移の臓器指向性や抗がん剤耐性メカニズム解析に今後活用されることが期待されます。 -
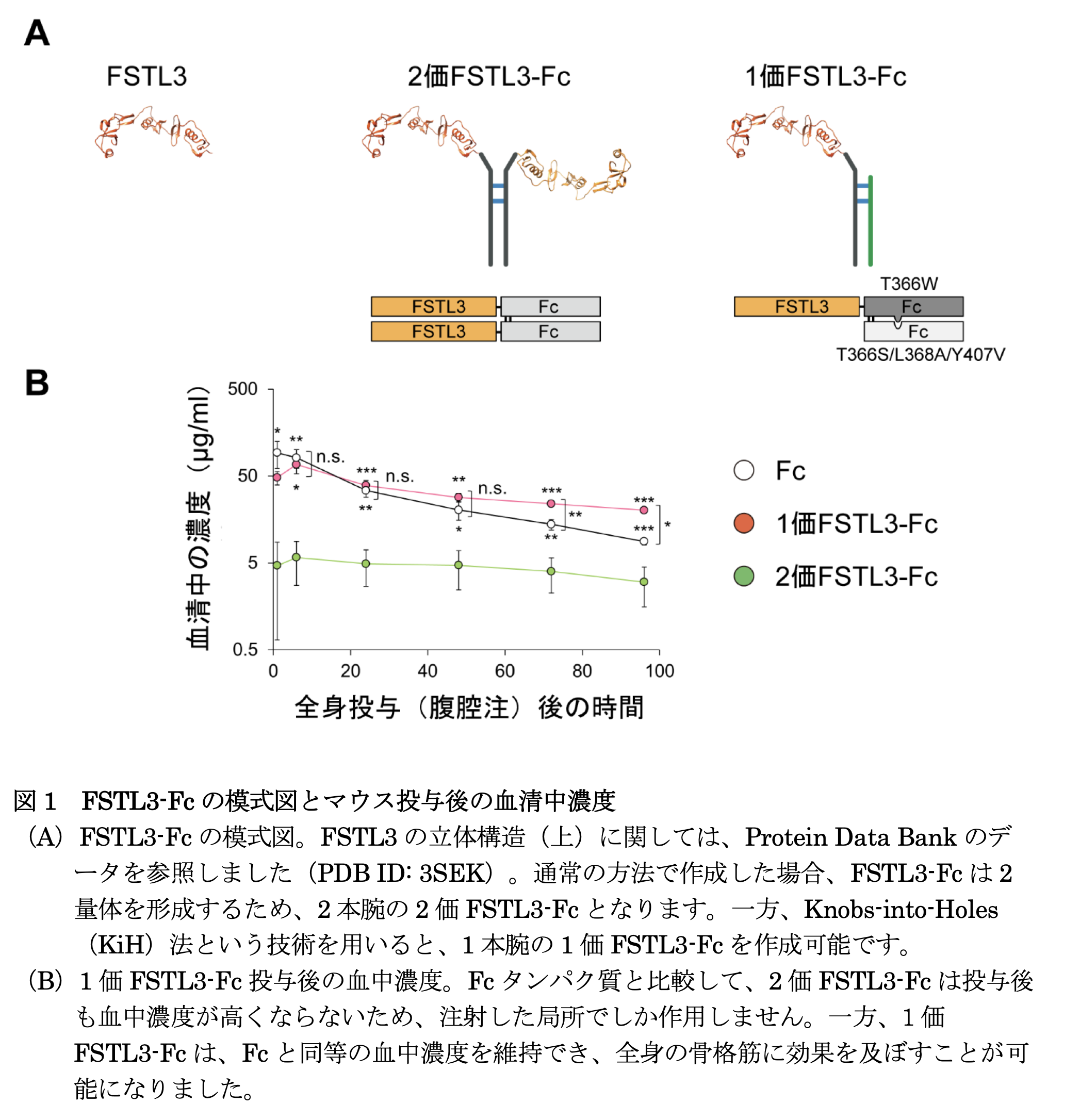 新規ミオスタチン阻害薬である 1 価 FSTL3-Fc の開発骨格筋の肥大や筋力の増大を促進するミオスタチン阻害薬の新規製剤として、1 価Follistatin-Like-3(FSTL3)-Fc を開発しました。 1 価 FSTL3-Fc は、標的と考えられる因子を過不足なく阻害し、マウスに投与した時に十分な効果が認められ、かつ先行製剤で問題となった副作用を認めませんでした。 有効でかつ副作用の可能性の低いミオスタチン阻害薬は、進行したがんで見られる悪液質や高齢者に見られるサルコペニア(骨格筋減弱症)などの骨格筋萎縮や神経筋疾患の治療薬として有望です。また骨格筋の持つ代謝機能を改善することで、肥満や 2 型糖尿病の治療にもつながることも期待されます。
新規ミオスタチン阻害薬である 1 価 FSTL3-Fc の開発骨格筋の肥大や筋力の増大を促進するミオスタチン阻害薬の新規製剤として、1 価Follistatin-Like-3(FSTL3)-Fc を開発しました。 1 価 FSTL3-Fc は、標的と考えられる因子を過不足なく阻害し、マウスに投与した時に十分な効果が認められ、かつ先行製剤で問題となった副作用を認めませんでした。 有効でかつ副作用の可能性の低いミオスタチン阻害薬は、進行したがんで見られる悪液質や高齢者に見られるサルコペニア(骨格筋減弱症)などの骨格筋萎縮や神経筋疾患の治療薬として有望です。また骨格筋の持つ代謝機能を改善することで、肥満や 2 型糖尿病の治療にもつながることも期待されます。 -
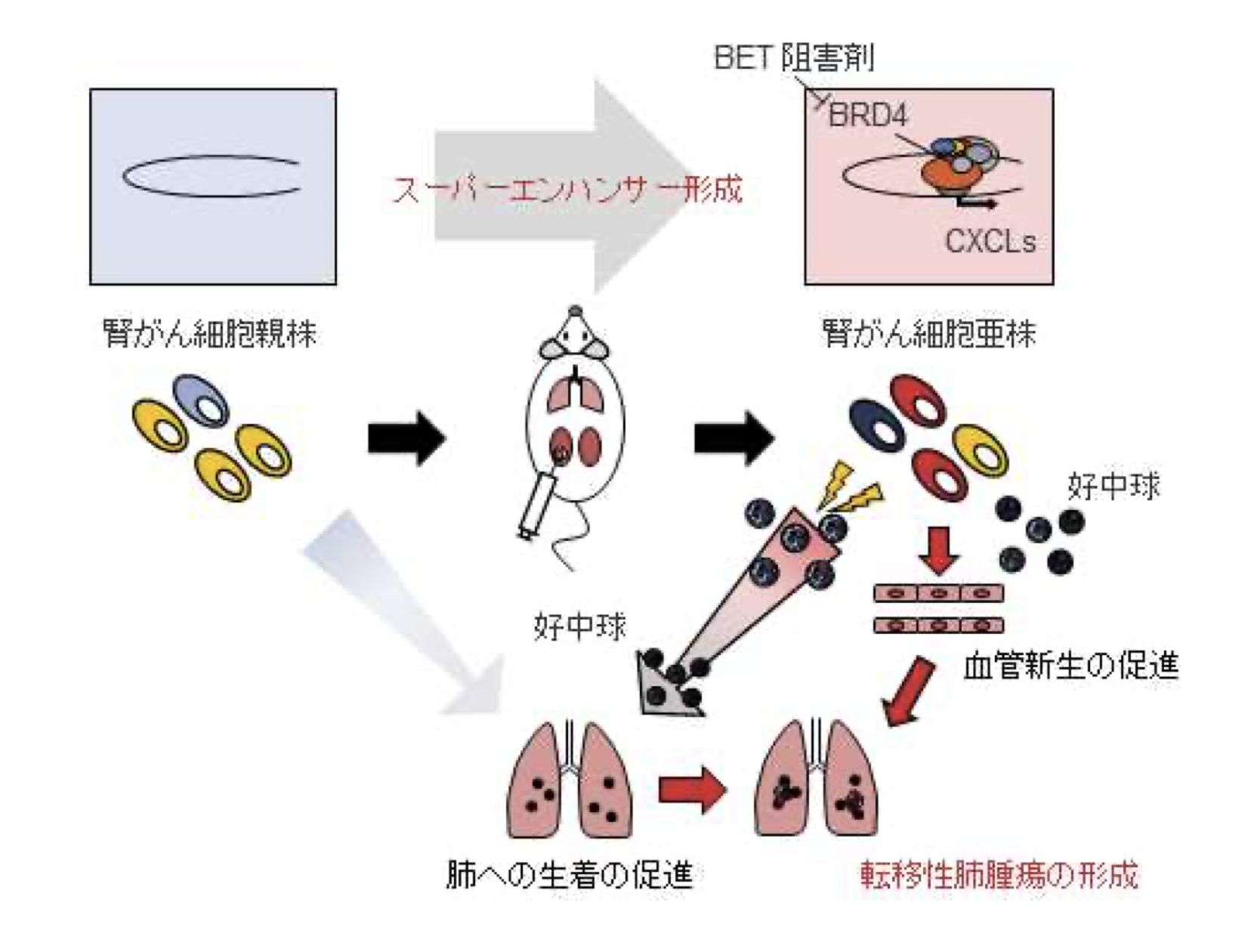 好中球を介した腎がん肺転移メカニズムの解明進行した腎がんでは、腎がん細胞は腫瘍内在性炎症を引き起こして好中球を活性化し、好中球の助けを得て肺に転移することが明らかになった。 腫瘍内在性炎症のメカニズムとして、スーパーエンハンサー形成などのエピゲノム制御機構によって、ケモカインが強力につくられていることが一因となることを見出した。 BET 阻害剤によりスーパーエンハンサーの活性を減弱させることで、腎がん細胞の肺転移が抑制されたことから、この薬剤が腎がんの新たな分子標的治療薬として期待される。
好中球を介した腎がん肺転移メカニズムの解明進行した腎がんでは、腎がん細胞は腫瘍内在性炎症を引き起こして好中球を活性化し、好中球の助けを得て肺に転移することが明らかになった。 腫瘍内在性炎症のメカニズムとして、スーパーエンハンサー形成などのエピゲノム制御機構によって、ケモカインが強力につくられていることが一因となることを見出した。 BET 阻害剤によりスーパーエンハンサーの活性を減弱させることで、腎がん細胞の肺転移が抑制されたことから、この薬剤が腎がんの新たな分子標的治療薬として期待される。 -
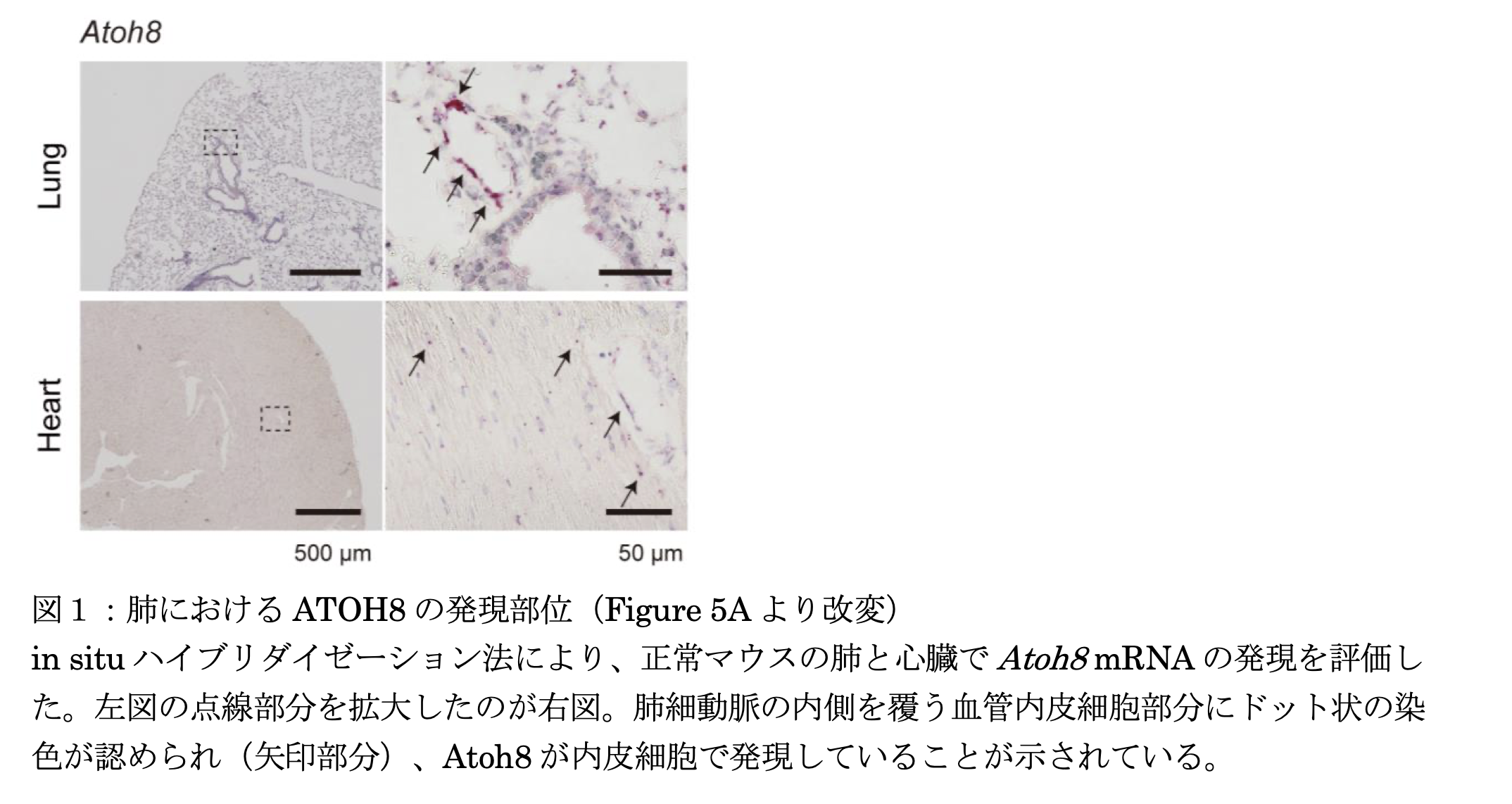 肺動脈性肺高血圧症の疾患関連遺伝子ATOH8の同定肺動脈性肺高血圧症(PAH)では、骨形成因子(BMP)の働きに異常があることが知られていたが、その発症メカニズムについては未だ不明な点が多い。 BMPシグナルの標的遺伝子の中で、転写因子 ATOH8 の機能を失ったマウスは肺高血圧症の症状を呈すること、培養細胞で ATOH8 が低酸素に対する細胞応答を調節することを明らかにした。 以上の結果より、肺動脈血管内皮細胞の BMP/ATOH8 経路は、低酸素に対して保護的役割を果たし、肺高血圧症の発症・進展に関わっていることが示唆された。
肺動脈性肺高血圧症の疾患関連遺伝子ATOH8の同定肺動脈性肺高血圧症(PAH)では、骨形成因子(BMP)の働きに異常があることが知られていたが、その発症メカニズムについては未だ不明な点が多い。 BMPシグナルの標的遺伝子の中で、転写因子 ATOH8 の機能を失ったマウスは肺高血圧症の症状を呈すること、培養細胞で ATOH8 が低酸素に対する細胞応答を調節することを明らかにした。 以上の結果より、肺動脈血管内皮細胞の BMP/ATOH8 経路は、低酸素に対して保護的役割を果たし、肺高血圧症の発症・進展に関わっていることが示唆された。 -
Mesenchymal 型神経膠芽腫に対する新規治療法の開発神経膠芽腫 (glioblastoma multiforme; GBM)は我が国では年間約 2200 人が発症する希少がんであり、近年の研究の進展にもかかわらず未だに著しい予後の改善が見られていない代表的な難治性がんである。GBM はいくつかのサブタイプに分類されるが、中でも mesenchymal 型(以下 MES 型)の GBM 細胞は放射線や化学療法などに治療抵抗性を示すことが知られている。我々は MES 型 GBM に特徴的に発現している遺伝子を探索し、HVEM (herpes virus entry mediator , 別名 TNFRSF14)を同定した。本研究ではヒトHVEM を標的とした 抗体を用いた非臨床試験を行い、ヒト HVEM 抗体の臨床応用を実現するために研究を推進している。